
基礎生物学研究所



2007.07.03
岡崎統合バイオサイエンスセンター/基礎生物学研究所の小林悟教授らは、精子をつくる幹細胞を維持する機構を世界にさきがけショウジョウバエで明らかにしました。幹細胞が維持されるために必要な細胞群は、生殖幹細胞ニッチ(ニッチ)と呼ばれています。本研究グループは、セブンレス(sevenless)という名の遺伝子に注目、この遺伝子の機能が精巣原基で失われるとニッチが異常に拡大することを明らかにしました。さらに、それに伴い幹細胞や精子に分化する途中の細胞が精巣中に過剰に蓄積され、精巣が腫瘍化することも明らかとなりました。ニッチおよび生殖幹細胞は、一生を通して精子が作られ続けるために必要ですが、これらの細胞が異常に増えると腫瘍化を引き起こすことが明らかとなったわけです。この危険性を回避し、正常に精子を作り続けるために、セブンレス遺伝子が必要であることが示されました。幹細胞は分化した細胞を供給する元となるもので、器官の成長や維持さらに再生時に重要な役割を果たします。一方、幹細胞数の異常な減少や増加は、腫瘍化など器官の正常な機能を妨げる要因になると考えられています。したがって、適正な数の幹細胞を維持する機構の解明は、生物学や医学の研究分野で特に注目されている研究課題です。幹細胞の維持には幹細胞と隣接するニッチと呼ばれる細胞群の働きが必須であることがいくつかの器官で知られています。しかし、ニッチそのものが発生過程で形成される機構についてはほとんど明らかにされていませんでした。本研究で得られた知見は、多くの器官におけるニッチや幹細胞の形成機構を明らかにする基盤となることが期待され、生殖・再生医療にもつながる可能性があります。本研究は、岡崎統合バイオサイエンスセンター/基礎生物学研究所の北舘祐研究員、小林悟教授らの研究グループにより行われました。研究の詳細は、2007 年7月3日に、米国の専門誌 デベロップメンタル セル(Developmental Cell)誌で発表されました。
一生を通して精子が作られ続けるためには、精子を供給する元になる生殖幹細胞が必要です。ショウジョウバエ成虫の精巣は、細長い袋状の構造をしており、その先端に生殖幹細胞が位置し、そこから後端にかけて連続的に精子形成が進行します。精巣先端の生殖幹細胞は分裂を繰り返し、分裂により生じた一方の細胞は再び生殖幹細胞となり、もう一方は精子へと分化する過程が繰り返されることで、連続した精子形成が進行します(図1)。この時、生殖幹細胞に隣接するハブ細胞と呼ばれる細胞群が、生殖幹細胞にシグナルを送り、分裂能力や未分化状態の維持といった生殖幹細胞の特殊な能力の維持を行っています。このような、幹細胞の性質を維持する環境をつくりだす細胞は特にニッチと呼ばれています。ハブ細胞、すなわち生殖幹細胞ニッチの果たす機能に関しては分子レベルでの研究が精力的に行われてきました。しかし、生殖幹細胞ニッチ自身が発生過程でどのように作り出されるかに関してはほとんど明らかになっていませんでした。
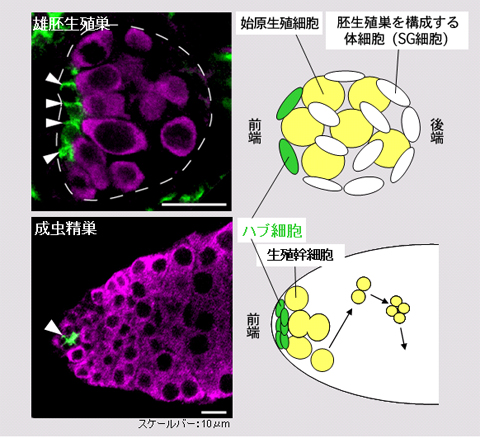 図1:雄の胚生殖巣および成虫の精巣におけるハブ細胞
図1:雄の胚生殖巣および成虫の精巣におけるハブ細胞
矢頭で示した緑の細胞がハブ細胞である。写真中ピンクで示される細胞は始原生殖細胞(上図)および生殖幹細胞と精子形成過程にある細胞群(下図)。
研究グループは、ショウジョウバエの精巣における生殖幹細胞ニッチであるハブ細胞の形成メカニズムを解明しました。精巣は、卵の中で胚発生が進行する時期に作られる胚生殖巣に由来します。胚生殖巣は、特殊な体細胞(SG細胞と呼ばれています)と生殖細胞の前駆細胞である始原生殖細胞から成っています。このうち胚生殖巣の前端部のSG細胞がハブ細胞に分化することが知られていました(図1)。しかし、なぜ前端部のSG細胞だけが、ハブ細胞に分化するのかという事はまったくの謎でした。研究グループは、これまでに胚生殖巣で発現する遺伝子を網羅的に同定する研究を行ってきました。同定された遺伝子の発現を調べていく過程で、胚生殖巣内の一部のSG細胞でのみ発現する遺伝子があることがわかってきました。そのような遺伝子の一つであるセブンレスの機能解析から、ハブ細胞の形成機構が明らかになったのです。セブンレス遺伝子は、雄胚生殖巣のSG細胞のうち、ハブ細胞に分化することのない後半部のSG細胞でのみ発現が観察されました(図2)。
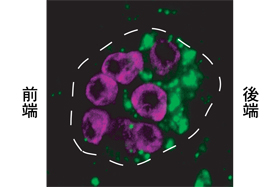 図2:セブンレス遺伝子の発現
図2:セブンレス遺伝子の発現
セブンレス遺伝子は雄胚生殖巣の後半部のSG細胞で発現する(図中の緑の部分)。ピンク色の細胞は始原生殖細胞。胚生殖巣を白い点線で囲んでいる。
このことから、研究グループはSG細胞がハブ細胞に分化する過程が、セブンレス遺伝子の働きにより抑制されているのではないかと考えたわけです。これを確かめるために、突然変異によりセブンレス遺伝子の機能を失わせたところ、通常はハブ細胞にはならない胚生殖巣後半部のSG細胞もハブ細胞に分化し、正常のものに比べ多くのハブ細胞が形成されることが明らかになりました(図3)。この結果から、当初の予想が正しいことがわかりました。さらに、このようなハブ細胞数の増加に伴い、生殖幹細胞の数も増加し、成虫の精巣中において精子形成をおこなっている細胞が過剰に蓄積されることもわかりました。このような細胞の過剰な蓄積により、成虫の精巣は腫瘍のように肥大化することも明らかになりました(図4)。以上のことから、セブンレス遺伝子は、ハブ細胞の数を制御することで、適正な数の生殖幹細胞を維持し、過剰な精子形成による腫瘍化を防ぐ役割があると考えられます。研究成果のもう一つのポイントは、始原生殖細胞からSG細胞への情報の受け渡しが、セブンレスの機能に必須であるという点です。セブンレス遺伝子は、情報を受け取る受容体型膜タンパク質をコードしています。セブンレス・タンパク質は、ボス(Boss)というタンパク質と結合することで活性化されます。ボス・タンパク質の分布を調べたところ、胚生殖巣内の始原生殖細胞で発現が観察されました。さらに、ボスの機能を欠く突然変異を持つ個体では、セブンレスの機能を欠くものと同様に、ハブ細胞数が増加することがわかりました(図3)。以上の結果を考えあわせると、始原生殖細胞で発現するボスにより、セブンレスが活性化し、胚生殖巣後半部のSG細胞がハブ細胞に分化するのを抑制すると結論づけられます(図5)。これは、始原生殖細胞から体細胞(SG細胞)へのシグナルの受け渡しを明らかにした初めての例であり、胚生殖巣内における細胞間の相互作用が生殖幹細胞ニッチの形成に重要な役割を持つことを示しています。
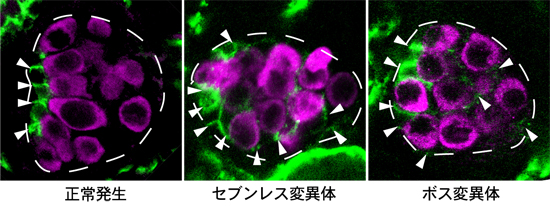 図3 左図:正常の胚生殖巣では、ハブ細胞(矢尻で示した緑色の細胞)は、胚生殖巣の前端部に形成される。中図:セブンレスの機能が失われると、ハブ細胞(矢尻:緑)は胚生殖巣の後半部にも形成される 右図:ボスの機能が失われた場合も、同じようにハブ細胞(矢尻:緑)は胚生殖巣の後半部にも形成される。胚生殖巣を白い点線で囲んでいる。白矢尻はハブ細胞を示す。図中、胚生殖巣は左が前端、右が後端になるように並べてある。
図3 左図:正常の胚生殖巣では、ハブ細胞(矢尻で示した緑色の細胞)は、胚生殖巣の前端部に形成される。中図:セブンレスの機能が失われると、ハブ細胞(矢尻:緑)は胚生殖巣の後半部にも形成される 右図:ボスの機能が失われた場合も、同じようにハブ細胞(矢尻:緑)は胚生殖巣の後半部にも形成される。胚生殖巣を白い点線で囲んでいる。白矢尻はハブ細胞を示す。図中、胚生殖巣は左が前端、右が後端になるように並べてある。
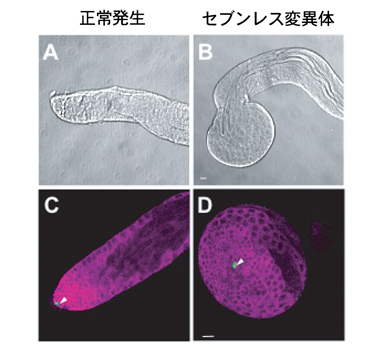
図4 正常な成虫精巣(AおよびC)とセブンレス遺伝子の機能を欠いた精巣(BおよびD)
セブンレスの機能を欠く精巣では、正常のものと比較し、精子形成過程の細胞が過剰に蓄積し、先端部が肥大している。
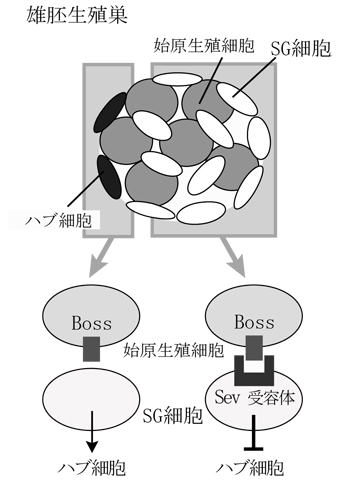 図5:雄の胚生殖巣中において、後半部のSG細胞で発現するセブンレス・タンパク質は、始原生殖細胞で発現するボス・タンパク質により活性化され、ハブ細胞への分化を阻害する。一方、先端部のSG細胞ではセブンレスが発現していないために、ハブ細胞に分化する。
図5:雄の胚生殖巣中において、後半部のSG細胞で発現するセブンレス・タンパク質は、始原生殖細胞で発現するボス・タンパク質により活性化され、ハブ細胞への分化を阻害する。一方、先端部のSG細胞ではセブンレスが発現していないために、ハブ細胞に分化する。
[今後の展望]
本研究で得られた知見は、生殖幹細胞ニッチに限らず、様々な組織の幹細胞ニッチの形成機構を明らかにする上で重要な基盤になると考えられます。また、将来的には、幹細胞ニッチのサイズを人為的に変えることで、幹細胞数を操作することも可能であり、生殖・再生医療分野への貢献も期待できます。
Developmental Cell (ディベロップメンタル・セル) 2007年7月2日号 (米国東部時間)
論文タイトル:
Boss/Sev Signaling from Germline to Soma Restricts Germline-Stem-Cell-Niche Formation in the Anterior Region of Drosophila Male Gonads
著者:
Yu Kitadate, Shuji Shigenobu, Kayo Arita and Satoru Kobayashi
本研究は、岡崎統合バイオサイエンスセンター/基礎生物学研究所 発生遺伝学研究部門の研究グループ(北舘祐 研究員、有田佳代 研究員、重信秀治 助手、小林悟 教授 )により実施されました。
本研究は、岡崎統合バイオサイエンスセンターと大阪大学蛋白質研究所との連携研究助成、および科学技術振興機構(CREST研究)からのサポートを受けて実施されました。
基礎生物学研究所 発生遺伝学研究部門
教授 小林 悟
Tel: 0564-59-5875(研究室)
E-mail: skob@nibb.ac.jp
URL: http://germcell.nibb.ac.jp/wp/
基礎生物学研究所 連携・広報企画運営戦略室
倉田 智子
Tel: 0564-55-7628
E-mail: press@nibb.ac.jp