
基礎生物学研究所



2013.05.31
岩手医科大学
自然科学研究機構 基礎生物学研究所
岩手医科大学解剖学講座木村英二助教と基礎生物学研究所生物機能解析センター亀井保博特任准教授ら研究グループは、赤外レーザー照射顕微鏡を用いて、ゼブラフィッシュの個体内で血管内皮細胞を対象に1細胞レベルで遺伝子発現を高効率に誘導することに世界で初めて成功した。本研究成果は、米国の科学雑誌『Arteriosclerosis, Thrombosis, and Vascular Biology』(2013年6月号)に掲載される。
研究グループでは、これまでいかにして血管系が個体内で形成されるか形態学的な手法を用いて明らかにしてきた。個体発生の過程で、血管系は決まったタイムコースに従い決まった形を作り上げていく。では、いかなるメカニズムによって、これらの形態形成過程は制御されているのか?この形態形成メカニズムを明らかにするためには、個体内で時間・空間的に1細胞レベルで目的遺伝子の発現を制御する必要があるが、既存の方法では十分にこれを達成することはできなかった。そこで一細胞で遺伝子発現誘導を可能にする赤外レーザー照射顕微鏡(IR-LEGO: infrared laser evoked gene operator)の開発グループと共同で新たな実験系の樹立を試みこれに成功した。IR-LEGOとは、赤外レーザーを照射することで局所的に細胞を温めて、熱ショックプロモーター下流の目的遺伝子の発現を誘導するシステムで、今回研究グループは、このシステムに血管内皮細胞の核で特異的に蛍光を発する遺伝子組み換えゼブラフィッシュを組み合わせることで、個体内の血管内皮細胞に効率よく赤外レーザーを照射し、遺伝子発現を誘導できるシステムを構築した。これまでのIR-LEGOではメダカやゼブラフィッシュなどの脊椎動物が対象の場合、1細胞レベルで効率よく遺伝子発現を誘導することは困難であったが、研究グループのシステムでは、条件を最適化することで最大で60%の効率で、標的細胞の遺伝子発現が誘導された。また蛍光タンパク質を誘導することで、特定の細胞を標識しその後の追跡が可能となるが、これにより脳と脊髄の血管系がどのようにしてつながっていくのか、その連結に関わる細胞を明らかにすることにも成功した。一方赤外レーザーの照射条件を変えることにより、瞬間的に細胞を破壊(焼却)することも可能となり、1細胞レベルで発生途中の血管内皮細胞を破壊し、その後の形態形成への影響を評価することにも成功した。特定の細胞を局所的に破壊する方法は、再生過程の解析にも有用となる。
血管はほぼすべての組織に含まれている。本研究成果を利用して血管系の形態形成メカニズムの理解が進むことで、将来的に再生医療やガン医療の進展に貢献することが期待される。今後は、形態形成に関与する遺伝子を選定し、本システムを用いてその機能解析を進めていく。
<お問い合わせ先>
岩手医科大学 解剖学講座 人体発生学分野
助教 木村英二
電話:019-651-5111(内線5831)
自然科学研究機構 基礎生物学研究所光学解析室
特任准教授 亀井保博
電話:0564-55-7630
参考資料
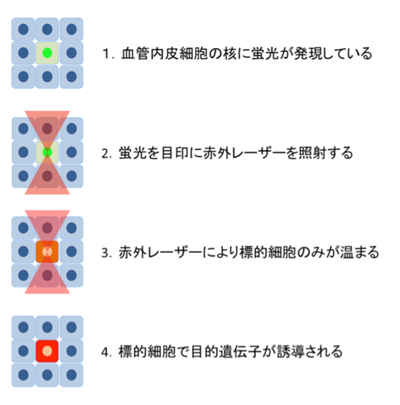
1)赤外レーザーにより単一標的細胞で遺伝子を発現誘導するメカニズム
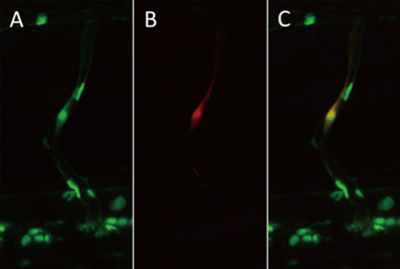
2)ゼブラフィッシュの個体内における遺伝子発現誘導
(単一の血管内皮細胞で蛍光タンパク質 mCherry の発現誘導に成功)
A) すべての血管内皮細胞の核で緑色蛍光タンパク質(EGFP)が発現している
B) 赤外レーザーにより単一の内皮細胞のみに赤色蛍光タンパク質の発現を誘導
C) AとBを合成したもの