自然科学研究機構 基礎生物学研究所
京都大学
ある種の上皮組織では、シート状に並んだ細胞が一定方向に揃った極性を持ちます。この極性は「平面内細胞極性(PCP)」と呼ばれ、神経管形成や内耳有毛細胞の配向などに見られます。脊椎動物ではPCPの形成に分泌性シグナルタンパク質であるWntが必要であることが示されており、その作用機構として、Wntは濃度勾配を形成し、個々の細胞がその濃度勾配の方向(勾配の傾き)を読み取ることで、PCPが揃えられるという説が提唱されてきました。
三井 優輔博士(前 基礎生物学研究所 助教・現 京都大学 医生物学研究所 助教)、鈴木 美奈子博士(前 基礎生物学研究所 大学院生/研究員・現 京都大学医生物学研究所 特定研究員)、および高田 慎治博士(前 基礎生物学研究所 教授・現 同名誉教授)らの研究グループは、アフリカツメガエル胚をモデルにWnt11によるPCP形成機構を詳細に検討しました。その結果、Wnt11はこれまでの説で想定されてきたような単純な濃度勾配を形成して分布するというよりも、むしろPCP因子とともに極性を持って細胞境界に局在していることを発見しました。このような偏った分布の形成にはWnt11とPCP因子が相互に必要であり、さらに、Wnt11とPCP因子が正のフィードバックを介して局所的に集積することにより細胞極性が自発的に生み出されることが示唆されました。また、この局所的な集積化においては、隣接する細胞間でPCP因子の非対称な集合が起こり、それをWntが安定化することも示され、隣接細胞間での極性の調整機構の一端も明らかになりました。
本成果は、発生を制御する分泌性シグナル分子の働きに関して、従来の概念であるトップダウン型だけではなく、むしろボトムアップ型の作用機構があることを明らかにしたものであり、平面内細胞極性の理解、さらには組織のパターン形成の理解を大きく前進させるものです。この成果は2026年2月25日付でScience Advances誌に掲載されました。
【研究の背景】
シート状の組織を構成する細胞が一定方向に揃った極性を持つことは発生における重要な現象であり、この極性は「平面内細胞極性(PCP)」と呼ばれます。PCPは神経管形成や内耳有毛細胞の配向などにおいて見られ、その破綻は二分脊椎などの重篤な発生異常の原因にもなります。身近なところでは我々ヒトの頭髪や体毛の流れもPCPによって細胞の方向性が揃っているからこそ見られるものです。PCPはコアPCP因子と呼ばれるタンパク質群(以下、PCP因子)が一つの細胞内で偏って分布するとともに隣接細胞間でその局在が連関することで作られています(図1)。
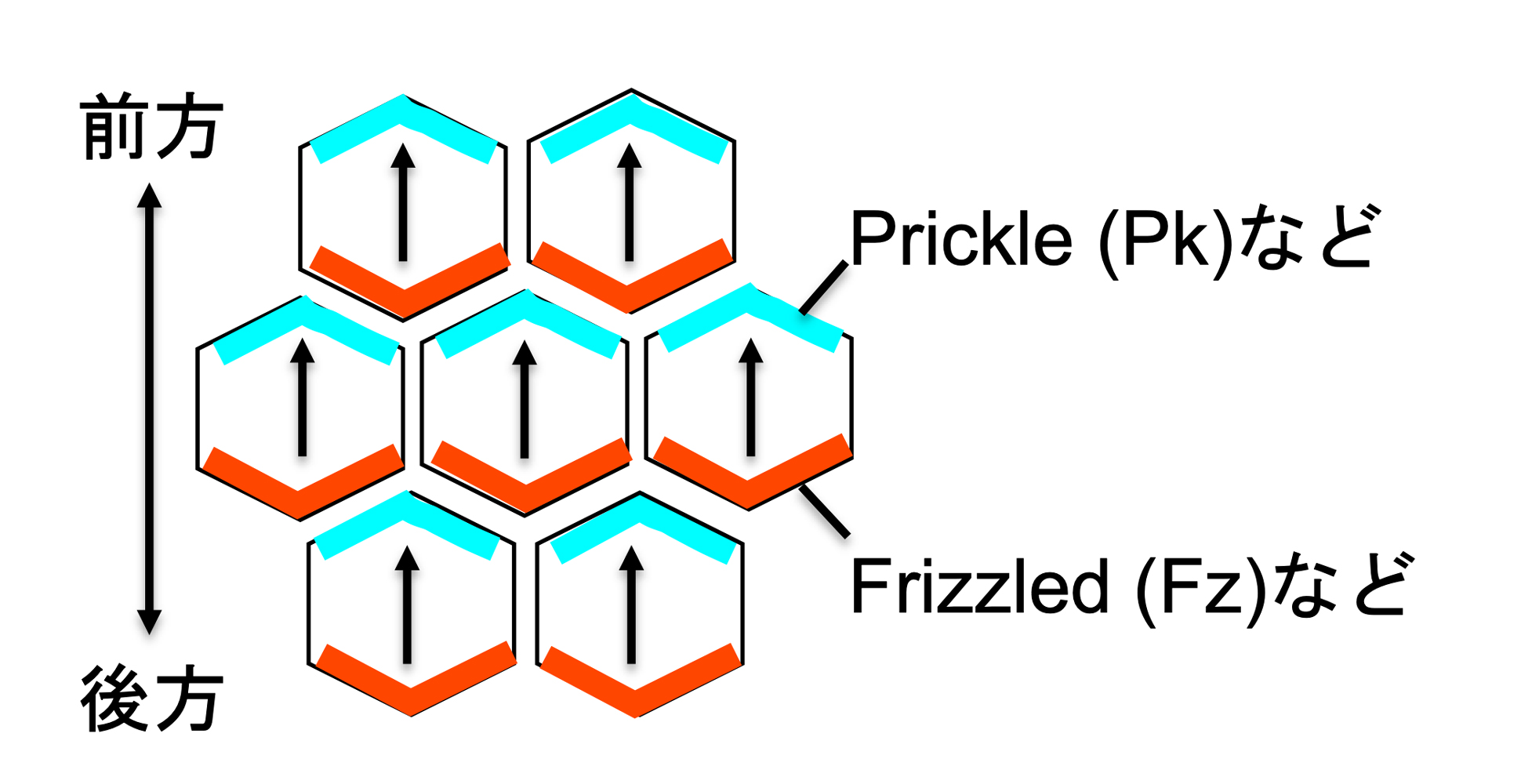
図1:PCP因子の局在による平面内細胞極性(PCP)の形成
Prickle (Pk), Frizzled(Fz)などのPCP因子は1細胞内でも片側に偏った分布を示し、細胞の方向性(矢印)を規定する。PkとFzは1細胞内では反対側に局在する一方、隣接細胞同士では近接した位置関係で、磁石のN極とS極に似たような挙動を示す。
脊椎動物においては、PCP因子の他に分泌性シグナルタンパク質のWntがPCPの制御に関わることが知られています。その際、Wntは濃度勾配を形成して分布し、組織内の個々の細胞が、濃度勾配の傾きを読み取ることで、細胞の方向性が揃うと考えられてきました。
しかしこの「濃度勾配説」にはいくつかの問題が考えられます。すなわち、組織の広い範囲をカバーする濃度勾配において、①一細胞分のわずかな濃度差を読み取れるだけの
感度が細胞にあるかという問題、また細胞が十分高感度であるならば濃度勾配は極めて滑らかかつ正確に作られなければなりませんが、②実際の胚の中での既知のWntの濃度勾配には
ノイズが多いという問題です(図2)。もし高感度な細胞がノイズの多い濃度勾配中に置かれると、部分的に方向性が逆転してしまう可能性が考えられます。つまり、分泌性シグナルの濃度勾配によって細胞の方向性を制御することは、生体内の制御系として簡単ではないことが予想されます。

図2:従来の「濃度勾配説」の問題点
そこで、三井らはPCPの制御に関わるWntの組織内分布について詳細に検討を行うことから、WntによるPCP制御機構の解析に取り組みました。彼らは実験的な操作が容易なアフリカツメガエル胚に着目し、PCPの制御に関わるWnt11の空間分布の詳細な観察を手がかりに研究を進めました。
【研究の成果】
1. Wnt11は濃度勾配を形成せず、PCP因子とともに偏った局在を示した。
アフリカツメガエル胚の神経板では、後方においてWnt11のmRNAが強く発現することから、「濃度勾配説」では、後方で濃く、前方で薄まる濃度勾配が想定されます。本研究で新たに作製した抗Wnt11抗体を用いて解析した結果、後方から前方への明瞭な濃度勾配は認められず、むしろWnt11は、PCP因子の局在に似て、左右方向の細胞境界に沿って偏在している(細胞の前後軸方向の辺には少なく、左右軸方向の辺に多い)ことがわかりました(図3)。そこで、PCP因子がWnt11の局在を制御する可能性を考えて、PCP因子の機能阻害実験および機能獲得実験を行った結果、Wnt11はPCP因子を制御しつつも、同時にPCP因子の偏りもWnt11を局在化させることを見いだしました。つまり、「濃度勾配説」では一方的にWnt11がPCPを制御すると思われていたが、実は両者は双方向的な制御関係だったのです。
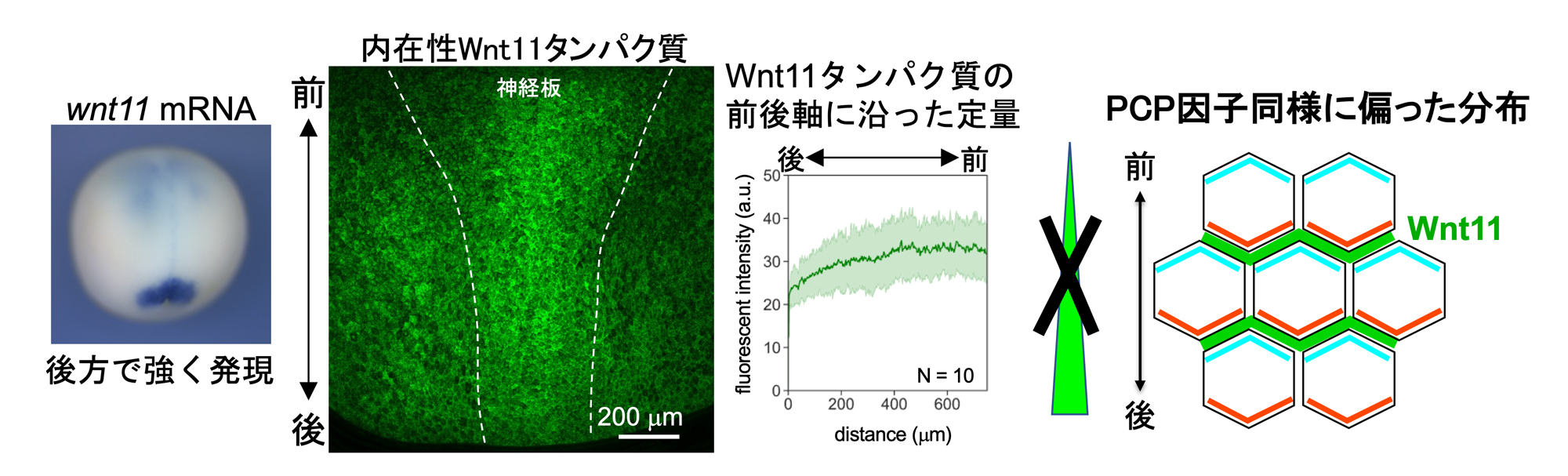
図3:アフリカツメガエル胚神経板における内在性Wnt11タンパク質の局在
2. Wnt11を均一に発現させるとPCP因子は自発的に偏ることを発見。また濃度勾配なしに細胞の方向を揃えられることを実験的に示した。
そこで、この双方向的な制御関係がPCP形成にどのように関わるのかを検討するために、人為的にPCPを操作する実験系に着目しました。内因性のPCPが弱いアフリカツメガエル胚動物極側のアニマルキャップと呼ばれる領域の一部にWnt11を局所的に過剰発現させ、さらにその周囲の細胞にPCP因子を異所的に発現させると、PCPを人為的に形成できることが知られています。この実験系を利用して、拡散しない「膜結合型」のWnt11を発現させ、細胞を極性化させる能力があるかを調べました。その結果、広い範囲の極性を揃える活性は失われましたが、隣接する細胞は極性化しました。一方、Wnt11を局所的には発現させずに、PCP因子とともに低濃度で発現させたところ、偏りの方向は組織内ではあまり揃ってはいないものの、個々の細胞ではPCP因子が強く偏っていました(ランダムな極性化)。また、Wnt11の濃度勾配が無くても、Wnt11とPCP因子の相互作用によってランダムな極性化が自発的に起きることがわかりました。
さらに、膜結合型Wnt11による隣接細胞の極性化と均一なWnt11によるランダムな極性化が起きる条件を組み合わせると、今度は広い範囲で方向が揃った極性化が見られました(図4)。この条件ではWnt11は濃度勾配を作ることなく、Wnt11を高発現する領域と低発現する領域の二領域があるだけですが、広い範囲の極性が揃うことが分かります。以上の実験結果とタイムラプス観察(動画)から、WntとPCP因子との相互作用により自発的に生まれるランダムな極性化が、Wnt高発現細胞からの誘導により方向性が揃った極性化へと進んで行くと考えるのが妥当であると結論されました。アフリカツメガエル胚の神経板ではWnt11は高発現領域と低発現領域の段差状の発現パターンを示しますが、ここで明らかにしたものと同様の仕組みで神経板においてもPCP形成が進むのではないかと推察できます。そして、このような仕組みで濃度勾配にまつわる厄介な問題(図1)を回避しているのかもしれません。
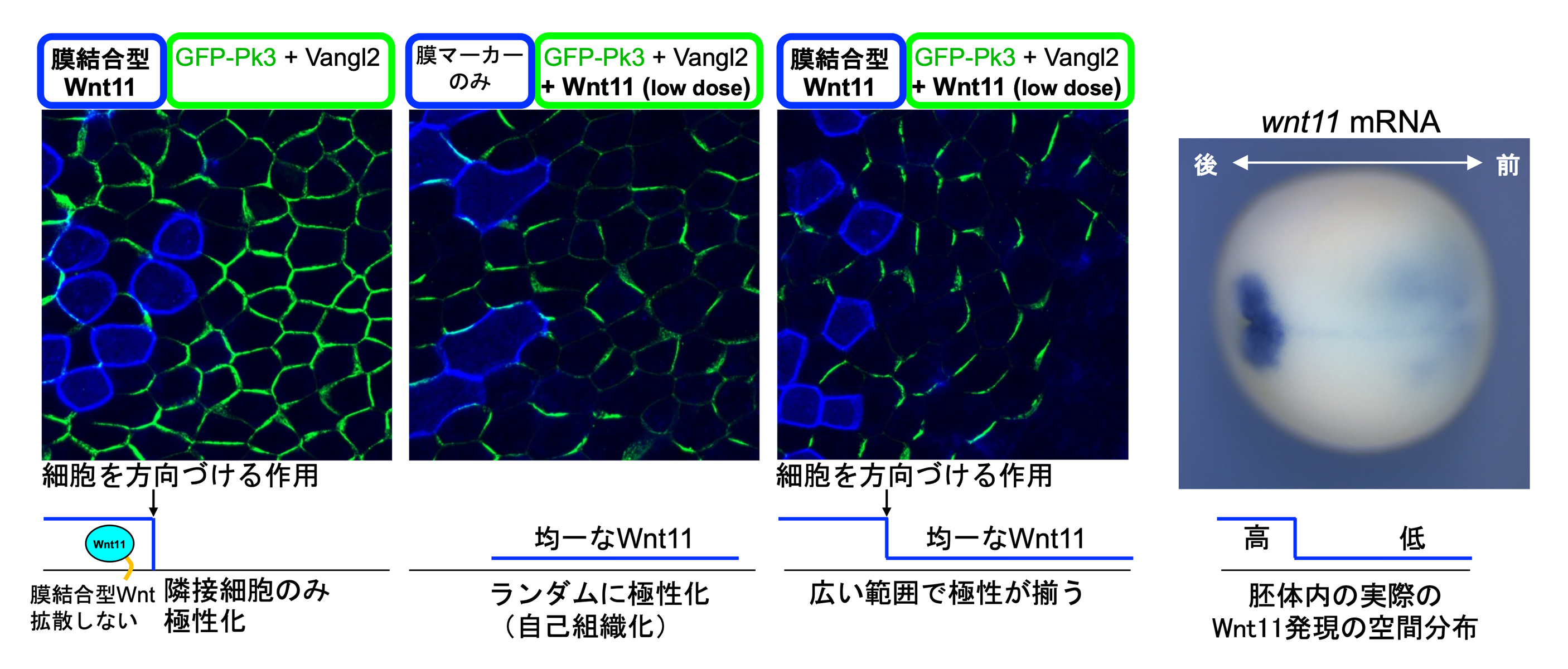
図4:Wnt11の高発現領域と低発現領域の存在が広い範囲での極性の揃いを引き起こす
動画:左下のマゼンタに光る細胞がWnt11を分泌しており、その作用によってPCP因子の一つを可視化するGFP-Pk3の局在がWnt11の分泌細胞の反対側の細胞辺へと偏っていく。このときPCPは20細胞以上と長距離にわたって揃うが、Wnt11の発現細胞に近い領域は早い時期から極性が揃うのに対して、遠い領域は時間的に遅れて極性が揃う。
3. Wnt11とPCP因子の相互制御のネットワークを明らかにし、細胞間を跨ぐPCP因子の「非対称な集積」を自発的に生み出すしくみを提案。
それでは、Wnt11とPCP因子の相互作用はどのようにして自発的な細胞の極性化を引き起こすのでしょうか?またどのようにしてPCP因子はWnt11の分布を偏らせるのでしょうか?三井らはWnt11を発現させると細胞辺上のPCP因子が濃く局在する細胞辺が現れることからWnt11は特定のPCP因子の組み合わせを安定化するのではないか、という仮説を立てました。その特定の組み合わせを考える上で、同じ細胞膜上、あるいは隣接細胞の細胞膜間でのPCP因子同士の位置関係は重要な情報です。超解像顕微鏡での解析からWnt11存在下ではPCP因子の一つであるVangl2のリン酸化がWntの受容体であるFrizzled7と同じ側で起こることを見いだし、これを手掛かりに、Wnt11がどのようなPCP因子の複合体を安定化させるかを体系的に検討しました。その結果、Wnt11とPCP因子のタンパク質間の安定化の制御ネットワークの存在を発見し、それによってPCP因子は隣接する細胞間で非対称な集積をするとともに、それをWntが安定化させることが示唆されました(図5)。さらに、このネットワークが正のフィードバック制御であることから、細胞を跨いだWnt11とPCP因子の集積は時間と共に亢進し、その結果自発的な極性化につながることが示唆されました。
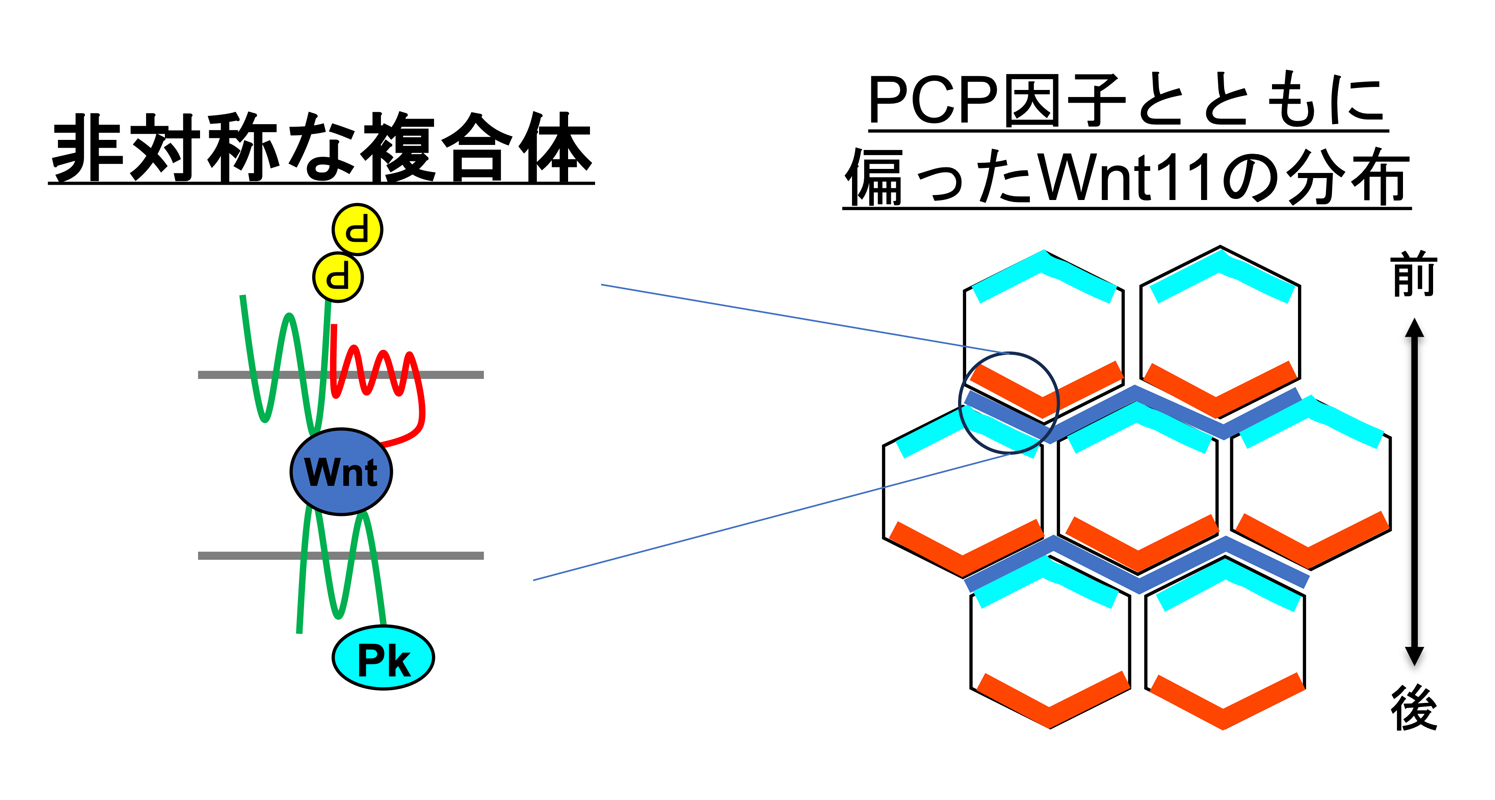
図5:細胞間を跨ぐPCP因子の「非対称な集積」を自発的に生み出すしくみを提案
【今後の展望】
本研究によってWntタンパク質が平面内細胞極性を揃える際の基本的なメカニズムを明らかにすることができ、20年以上解かれていなかった大きな問題を解決できたと言えます。この成果を元に、現在は生体外での構築が困難な平面内細胞極性を生体外で構築する手法の開発や平面内細胞極性に関連した疾患の理解も進むと期待されます。
【発表雑誌】
雑誌名 Science Advances
掲載日 2026年2月25日
論文タイトル: Planar cell polarity emerges through polarized accumulation of Wnt11
著者:Yusuke Mii (三井 優輔), Minako Suzuki(鈴木 美奈子), Hiroshi Koyama(小山 宏史), Kei Nakayama (中山 啓), Ritsuko Takada(高田 律子), Tomoe Kobayashi(小林 朋絵), Motosuke Tsutsumi(堤 元佐), Tomomi Nemoto(根本 知己), Makoto Matsuyama(松山 誠), Toshihiko Fujimori(藤森 俊彦), and Shinji Takada(高田 慎治)
DOI:
https://doi.org/10.1126/sciadv.aea0326
【研究グループ】
本研究は、自然科学研究機構 生命創成探究センター 兼 基礎生物学研究所 分子発生学研究部門(三井 優輔、鈴木 美奈子、高田 律子、高田 慎治)および京都大学 医生物学研究所(三井 優輔、鈴木 美奈子)を中心とし、基礎生物学研究所 初期発生研究部門(小山 宏史、藤森 俊彦)、重井医学研究所(小林 朋絵、松山 誠)、自然科学研究機構 生命創成探究センター 兼 生理学研究所(堤 元佐、根本 知己)、神戸薬科大学(中山 啓)からなる研究グループによる研究成果です。
【研究サポート】
本研究は、以下をはじめとする研究費の支援を受けて行われました。
科学研究費助成事業(18H02454, 21H02498, 24111002, 17H05782, 19H04797, 15K14532, 18K14720, 22H02637/23K23900, 23H04930, 22KJ1425 24K23205)、 JSTさきがけ(JPMJPR194B)、自然科学研究機構・若手分野間連携プロジェクト、自然科学研究機構・分野融合型共同研究事業(01112010)
【本研究に関するお問い合わせ先】
基礎生物学研究所
名誉教授 高田 慎治
TEL: 0564-59-5243
E-mail: stakada@nibb.ac.jp
京都大学 医生物学研究所
助教 三井 優輔
【報道担当】
基礎生物学研究所 広報室
TEL: 0564-55-7628
FAX: 0564-55-7597
E-mail: press@nibb.ac.jp
京都大学 広報室 国際広報班