
基礎生物学研究所



2010.05.27
通常、血中ナトリウム(Na)レベルは145mM付近に厳密に保たれています。例えば、絶水状態が長時間続くと体液中のNaレベルが上昇しますが、この状態で水と塩水を同時に提示されると、水を大量に摂取すると共に塩分摂取を回避します。また、抗利尿ホルモン(anti-diuretic hormone; ADH)であるバソプレッシンの脳下垂体後葉からの分泌量が増加し、排尿に伴う水分流出が抑えられます。こうした制御は脳内のセンサー分子群により体液の浸透圧やNaレベルが感知され、その情報が水分/塩分摂取行動の制御に関わる神経回路やバソプレッシン産生細胞へ送られることにより実現されています。この制御機構が何らかの理由で破綻すると体液Naレベルに恒常的な異常が現れます。基礎生物学研究所の野田昌晴教授らは、これまでの研究で電位依存性Naチャンネルと相同性のある分子Naxが体液Naレベルセンサーであることを明らかにしていました。血中Naレベルが恒常的に高くなる疾患は本態性高Na血症(essential hypernatremia)と呼ばれます。脳腫瘍形成や外傷によりバソプレッシン産生細胞のある脳内視床下部領域が損傷を受けてバソプレッシンの分泌能が低下したことが病因であることが多いことが知られています。しかし、核磁気共鳴画像法(MRI)を用いて検査を行っても著明な脳の異常が見当たらない症例もあり、その場合は原因不明とされてきました。野田昌晴教授らは、そのような原因不明の本態性高Na血症の一症例を解析したところ、患者の体内でNaxに対する自己抗体が産生されていたことを見出しました。この成果は、2010年5月27日に米国科学専門誌ニューロンにて発表されました。
・脳内に著明な損傷が見られず発症機構が不明であった本態性高Na血症の発症機構が説明され、新たな治療法につながる発見。
患者(入院時6歳6カ月)は、高Na血症を認め、緊急入院しました。血中Naレベルは輸液により一時的に正常値近くに回復しましたが、輸液を中断すると再び上昇したことから、本態性高Na血症と診断されました。そこで、頭部MRI 検査を実施しましたが、著明な異常が見つかりませんでした。その後、1日あたり1500ml以上の飲水によって血中Naレベルを正常値近くに維持しています。
入院後、副腎近傍に腫瘍が見つかり摘出しました。腫瘍摘出後も高Na血症の症状は消失しませんでした。口渇感がなく、抗利尿ホルモンであるバソプレッシンの分泌が低下していました。患者血液を調べたところ、Naxに対する自己抗体を産生していることがわかりました。また、腫瘍を調べると、Nax(体液Naレベルセンサー分子)を発現する細胞が異常増殖していました。
患者の血液からNaxに対する自己抗体を含む免疫グロブリンを分離し、マウスに投与しました(疾患動物モデルの作製)(図1)。患者の免疫グロブリンを投与されたマウスは1週間後には飲水量が低下するとともに、水摂取を制限した条件下(脱水状態)でもナトリウム摂取を抑制せず、バソプレッシンの分泌量(正常ならば脱水状態で増加する) の増加が弱いことから、尿量抑制による体内からの水分喪失の抑制が不充分となりました。その結果、患者と同様の高Na血症を発症しました。
脳弓下器官や終板脈管器官にはNaレベルセンサー(Nax)の他に浸透圧センサーなども発現しており、室傍核や視索上核におけるバソプレッシンの産生・下垂体への分泌を制御しています(図2)。脳弓下器官・終板脈管器官(図2赤丸)において抗Nax自己抗体の結合に伴って補体反応(下記注参照)が起き、Nax発現細胞が細胞死を起こしていることが判明しました。その出力であるバソプレッシン分泌制御経路(図2赤実線)や飲水行動/塩分摂取行動制御経路(図2赤点線:未解明)が正常に機能しなくなったと考えられます。
今回の知見は、末梢における神経節細胞腫の形成がNaxチャンネルを標的分子とする自己免疫性の神経疾患を誘発し、本態性高Na血症が引き起こされることを示しています。脳内に著明な損傷が見られず発症機構が不明であった本態性高Na血症の少なくとも一部の症例に関して発症機構を説明するものであり、新たな治療法の確立が期待されます。
注)補体反応:抗体が標的である抗原に結合した後、抗原抗体複合体に補体が結合、活性化する。その後、多くの補体成分が連鎖的に反応し、最終的に、抗体が結合した標的細胞に細胞死を誘導する。今回の症例では抗Nax自己抗体がNax発現細胞を攻撃した。
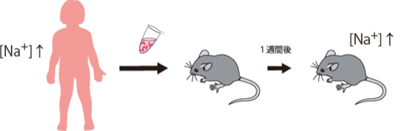
図1:疾患動物モデルの作製
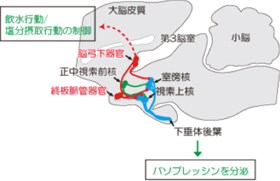
図2:マウス脳の縦断面図
米国科学専門誌 Neuron(ニューロン)2010年5月27日号掲載
論文タイトル:
"Autoimmunity to the sodium-level sensor in the brain causes essential hypernatremia"
「脳のナトリウムレベルセンサーに対する自己抗体産生が本態性高ナトリウム血症の原因となる 」
著者:Takeshi Y. Hiyama, Shinichi Matsuda, Akihiro Fujikawa, Masahito Matsumoto, Eiji Watanabe, Hiroshi Kajiwara, Fumio Niimura, Masaharu Noda
本研究は、基礎生物学研究所 統合神経生物学研究部門の野田昌晴教授と檜山武史助教らと、東海大学医学部小児科の新村文男准教授と松田晋一講師らの共同研究です。
本研究は、文部科学省科学研究費補助金のサポートを受けて行われました。
基礎生物学研究所 統合神経生物学研究部門
教授 野田 昌晴(ノダ マサハル)
Tel: 0564-59-5846(研究室)
E-mail: madon@nibb.ac.jp
助教 檜山 武史(ヒヤマ タケシ)
Tel: 0564-59-5848(研究室)
基礎生物学研究所 広報国際連携室
倉田 智子
Tel: 0564-55-7628
E-mail: press@nibb.ac.jp