多様性生物学研究室
研究の概要
生命現象の背後に潜む法則を数理で理解する
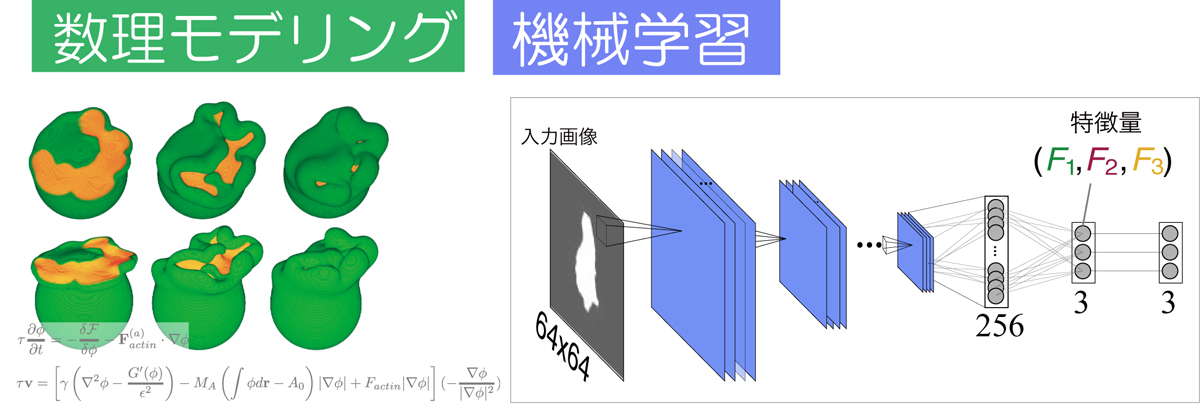
動的な生命現象の背後にどのようなメカニズムや因果が潜んでいるのか、どのように分子や細胞の集団から複雑で多様な運動が自己組織化してくるのか、これらを統合的に理解するには数理モデリングによるアプローチが重要となる。特定の遺伝子や分子に現象の原因を求めるのではなく、数理モデリングや機械学習解析を通して様々な生物種に共通する普遍的性質の理解を目指す。
細胞膜ダイナミクスのモデリング
脂質二重層から成る細胞膜は、分子の膜局在やアクチンフィラメントの重合、分子モーターの作用などにより時に動的に変形する。特にエキソ/エンドサイトーシスでは、形のトポロジーが変わるほどの劇的な変形が現れる。それらの変形に関わる重要な遺伝子・分子の解明は進んできたが、シグナル因子と協働してどのように細胞膜が特定の形状に自己組織化するのかという理解は十分ではない。
これらの問題に対し、細胞膜上のシグナル因子の反応拡散現象と細胞膜の変形をモデリングし、細胞変形の基本原理を解明することを目指している。これまでのところ細胞遊走に付随する2次元的な細胞変形のモデリング、マクロピノサイトーシスなどのエンドサイトーシスの3Dシミュレーションなどを行なっている。同時に機械学習を応用し、細胞の形状を計量、実験とシミュレーション結果をシステマティックかつ客観的に比較する手法を開発している(上図)。
多細胞シミュレーション手法の開発
発生過程や組織形成、創傷治癒などに代表される不均一な細胞集団から成る多細胞動態では、多様な細胞が複雑に相互作用し合い集団としての機能を果たす。このような状況で細胞の移動、変形、分裂/消滅、がどのように組織全体の変形と関係するのか、細胞スケール(ミクロ)と組織スケール(マクロ)を跨いだ解析は発展の途上にある。近年、実験技術やデータ解析技術は飛躍的な発展を遂げたが、現象の背後にあるメカニズムや因果の理解は不十分であり、これらを統合する数理モデリングによるアプローチが重要となる。
現在、フェイズフィールド法と呼ばれる数値計算手法を用いて、細胞性粘菌の集団運動を対象として多細胞モデリングを行なっている(図1左)。同時に、数千細胞のシミュレーションを可能にする理論的フレームワークも開発している(図1右)。
細胞内化学反応や分子ダイナミクスのモデリング
細胞内で起こる化学反応ではしばしば、反応に関与する分子の数が少数になることがありうる。こうした状況では分子の離散性・少数性に起因する確率性が無視できなくなり、従来の反応速度論的描像が破綻する。この少数性効果の基礎理論の構築や、キネシンによる協同的な微小管輸送現象への応用などを進めている。
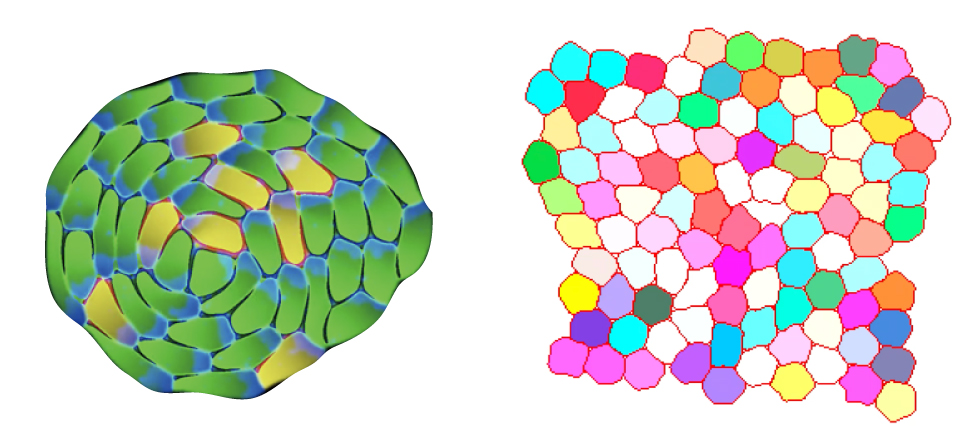
図 1. 多細胞動態のシミュレーション
多細胞フェイズフィールドシミュレーション(左)と細胞輪郭のフーリエ展開を基礎とした多細胞モデル(右)。
参考文献
Yamagishi, J.F., Saito, N. and Kaneko, K. (2020). Advantage of Leakage of Essential Metabolites for Cells. Phys. Rev. Lett. 124, 048101.
Saito, N. and Kaneko, K. (2017). Embedding dual function into molecular motors through collective motion. Sci. Rep. 10, 44288.
Saito, N., Sughiyama, Y. and Kaneko, K. (2016). Motif Analysis for Small-Number Effects in Chemical Reaction Dynamics. J. Chem. Phys. 145, 094111.
Saito, N., Kaneko, K. (2015). Theoretical Analysis of Discreteness-Induced Transition in Autocatalytic Reaction Dynamics. Phys. Rev. E 91, 022707.







