
基礎生物学研究所




生物は祖先が持っていなかった新しい形質を次々と生み出しながら進化してきました。そして、新規形質の多くは、いくつかの性質が整って初めて有利になるような複合形質です。新規複合形質はランダムな突然変異の蓄積だけで説明できるのでしょうか。あるいは未知の進化機構が存在しているのでしょうか。この問題を解くには、新規複合形質を遺伝子のレベルに還元し、それらができあがるメカニズムを解明し、さらに、近縁種との比較から進化過程を推定することが必要です。我々は、モデル植物を用いた研究に加え、ゲノム解読とゲノム改変技術の革新を助けに、非モデル植物をモデル植物化し、(1)電気信号やカルシウムシグナルを介した植物の速い情報伝達、(2)体細胞から多能性幹細胞へのリプログラミング、(3)食虫植物など陸上植物の発生と形態を個別な研究対象として、それらから得られた結果を総合し、新規複合形質がどのように進化しうるかのメカニズムを描き出すことを目指しています。(詳細は https://www.nibb.ac.jp/evodevo)。

植物の中には、速く動けるように進化した種がある。食虫植物ハエトリソウは、獲物が葉の上の感覚毛を30秒以内に2回触ると、瞬時に葉を閉じる。同じく食虫植物のモウセンゴケは、粘液を分泌した触毛を動かし数分で獲物を捕らえる。オジギソウは、昆虫などの捕食を避けるため、秒速で葉を閉じる。神経や筋肉の無い植物が、どうしてこのように速く反応できるのだろうか。約150年前、進化論のチャールズ・ダーウィンは、これらの植物について先駆的な研究を行い、さらに、その後の多くの研究の積み重ねから、刺激に伴い、動物の神経と同じように電気信号が検出されることがわかってきた。しかし、どんな分子がどんな仕組みでどんな経路で電気信号を送っているのかは、未だにわかっていない。これらの奇妙な植物では遺伝子を調べる方法が確立されていなかったからだ。我々は、これら3種のゲノム配列を解読し、さらに、遺伝子導入技術によってゲノム改変することに成功した。電気信号に関わると考えられているカルシウムイオンを可視化するとともに、刺激の受容や伝播に関わる組織で働いている遺伝子を破壊したり、他の組織で働かせたりすることで、接触刺激の受容と伝播の仕組みを解明しようとしている。そして、これらの植物と普通の植物を比較することで、植物の高速情報伝達の仕組みがどのように進化してきたのかを推定したい。
食虫植物のフクロユキノシタは、消化液のたまった壺型の捕虫葉を形成し、小動物を捕獲して栄養を得ている。捕虫葉は、通常の植物の平面葉から進化してきた。しかし、どんな遺伝子がどのように変わることで進化したかはわかっていない。これまでの研究から、発生初期段階で特定の場所の細胞分裂が変化することで大きな形態進化が起きた可能性があることがわかり、検証を進めている。
我々がヒメツリガネゴケで発見したステミンSTEMINという遺伝子は、単独で、分化した葉細胞を幹細胞に変化させることができる。ステミンは転写因子であるが、それ以外に、クロマチン修飾やDNA損傷と関連して幹細胞化の未知の分子機構を担っているらしいことがわかってきた。ステミンを介した幹細胞化の分子機構解明から、植物が動物より幹細胞化しやすい仕組みの解明を目指す。
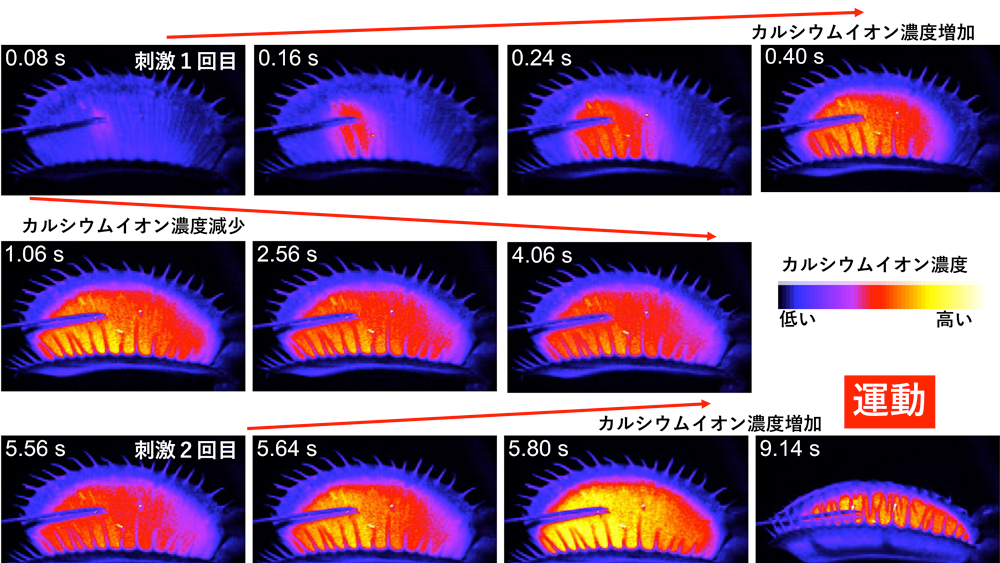
図1. カルシウムイオン量の変化を可視化した遺伝子組換ハエトリソウ。30秒以内に2回感覚毛を刺激すると葉が閉じるが、カルシウムが記憶物質として機能し、閾値を超えると葉が閉じる。
上記研究内容に関連する共同研究を歓迎します。
長谷部 光泰 教授 E-mail: mhasebe@nibb.ac.jp
