研究内容
マウス精子形成幹細胞の正体とニッチをさぐる
 ほ乳類の精巣では、少数の幹細胞が自分自身を保存(自己複製)しながら、分化細胞の精子を生み出し続けます。これを支える精子幹細胞は、世代を超えて遺伝情報を伝達する重要な細胞ですが、その実体は謎に包まれています。生殖細胞研究部門では、独自に開発したさまざまな実験系を活用して、マウス精子幹細胞の性質と挙動を一つ一つ解き明かし、幹細胞の真の姿を垣間みようと、いくつかの切り口から研究を行っています。
ほ乳類の精巣では、少数の幹細胞が自分自身を保存(自己複製)しながら、分化細胞の精子を生み出し続けます。これを支える精子幹細胞は、世代を超えて遺伝情報を伝達する重要な細胞ですが、その実体は謎に包まれています。生殖細胞研究部門では、独自に開発したさまざまな実験系を活用して、マウス精子幹細胞の性質と挙動を一つ一つ解き明かし、幹細胞の真の姿を垣間みようと、いくつかの切り口から研究を行っています。
幹細胞は、どんな素顔を見せてくれるでしょうか?
背景:マウス精子形成とその幹細胞
私たちが対象としている「幹細胞」は、ES細胞やiPS細胞、あるいは造血幹細胞のような、多分化能(複数の細胞種に分化する能力)を持つ細胞ではありません。ほ乳類の「精子幹細胞」は精子にしか分化しませんが、長いものでは何十年にもわたって精子形成を支えるおおもとの細胞です。
マウスの精子形成は、精巣の中の精細管と呼ばれる長い管の中で起こります(図1)。減数分裂に入る前に体細胞分裂をする段階の細胞(精原細胞)は、精細管を囲む基底膜の上に位置しています。その後、減数分裂過程の精母細胞、半数体となった精子細胞と、分化の進行とともに内腔に向かって移動して行きます。精原細胞のうちのごく少数の細胞が幹細胞として機能することは明らかですが、幹細胞の正体は未だ明らかになっていません。1994年、移植による幹細胞の機能アッセイが開発され、その後「未分化型精原細胞」と呼ばれる少数の細胞が幹細胞を含むことが明らかとなりました。では、「未分化型精原細胞」のうち、どの細胞が、どこで、どのような制御を受けることによって、幹細胞としての機能を発揮するのでしょうか?固定した標本の解析からこの問題に対しての最終的な答えを得るのは、原理的に不可能です。
また、「幹細胞は自己複製と分化を行い、組織のホメオスタシスを維持する。」と言われますが、今日の幹細胞研究の多くが、組織再生や移植、試験管内のコロニー形成を解析しており、組織で実際に自己複製する「幹細胞」を研究している例は決して多くはありません。我々は、時間を越えた細胞の挙動を解析する実験系(ライブイメージングやパルス標識実験)を駆使して、実際に組織の中で機能する幹細胞の真の姿を明らかにすることに挑戦しています。
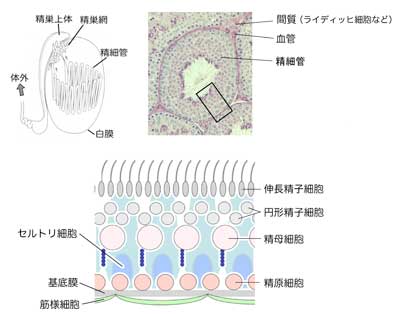
図1 マウス精巣の構築
(A)精子形成の場である精細管は、複雑に折りたたまれている(1本の精細管のみ示す)。(B)精細管の断面(PAS-ヘマトキシリン染色)。多数の細胞がぎっしりと詰まっている。幹細胞を含む精原細胞は基底膜(周囲の赤い線)上にあり、分化に伴い内側に移動する。内腔に面して成熟した精子細胞が見られる。精細管の間の3角形の部分を、血管とその周囲の間質が充たしている。(C)精細管の断面の模式図(Bの四角の部分に相当)。
1.精子幹細胞の正体に迫る
マウス精巣に見られる生殖細胞の中で、形態的に最も未熟とされるものは、通常の細胞と同じくただ一つの核を持つ「As細胞」です。As細胞が分化しながら数を増やす時、娘細胞同志がつながったままで残り、2、4、8、16・・・個の細胞がつながったシストを形成します(図2)。従来、「Asだけが幹細胞であり、シストとなった細胞は不可逆的に分化へと運命付けられている」と信じられて来ました。1971 年に提唱された「Asモデル」です(図2)。
しかし、我々がおこなったライブイメージングの結果、16個程までの比較的短いシストが断片化し、より未分化な細胞に戻る場合があることを発見しました(図3)。これは、「真の幹細胞の可能性が最も高いAs細胞だけではなく、更に多くの細胞(ポテンシャル幹細胞)を加えた細胞が集団として幹細胞システムを支えている」ことを示唆します。ポテンシャル幹細胞は、真の幹細胞とは違って分化に方向付けられているものの、自己複製する潜在能力を維持しています。「真の幹細胞」のバックアップとして、安定した精子形成を維持する上で重要な機能を果たしていると考えられます。断片化や分化の方向を制御する機構の解明が現在の課題です。
Nakagawa et al., Developmental Cell, 2007
Nakagawa et al., Science, 2010
プレスリリース
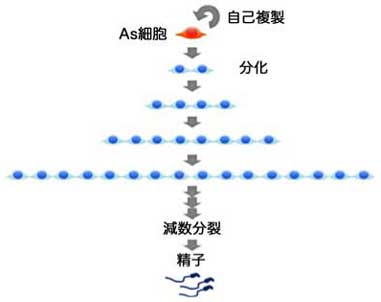
図2 マウス精子幹細胞の定説「Asモデル」
As細胞のみが自己複製する幹細胞であり、合胞体を作る2、4、8、16・・・の細胞は不可逆的に分化に運命づけられているとする。
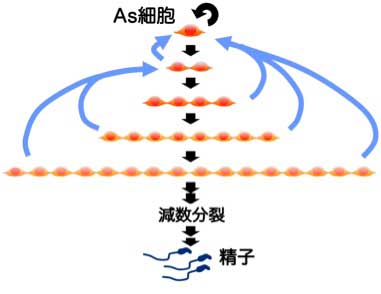
図3 明らかとなってきた可逆的でしなやかな幹細胞システム
Asモデルで想定された自己複製と不可逆的な分化(黒矢印)に加え、分化に向かった合胞体細胞が断片化して、より未分化な細胞に戻る(青矢印)ことにより、これらの細胞が集団として幹細胞システムを形成している。
2.精子幹細胞は次々と入れ替わる
大切な遺伝情報を持つ「精子幹細胞」は厳密に「非対称分裂」を繰り返し、精巣の中で一つ一つ大切に守られていると、当然のように信じられて来ました(図4)。私たちは、パルス標識した精子幹細胞の運命を1年以上にわたって追跡しました。その結果は驚くべきものでした。一つ一つの幹細胞は決して特別に守られている訳ではなく、平均してわずか1〜2週間の寿命しか持たず、次々と消滅していたのです。そして、失われた幹細胞は、隣の幹細胞から生まれた細胞によって補充されていました。更に、数学的解析の結果は、どの幹細胞が消えてどの幹細胞が生き残って増えていくかは、偶然に(確率論的に)決まることを示していました。このように、幹細胞のグループがお互いに入れ替わりながら自らの集団を維持すると同時に精子を作る細胞を供給しているという、新しい幹細胞の姿が明らかになって来ました(図5)。オリジナルの幹細胞だからといって特別扱いされて守られているのではなく、オリジナルが失われるとコピーによって補充されます。そして、オリジナルの幹細胞もコピーして作られた幹細胞も区別なく、同じ「幹細胞」として働いているのです。興味深いことに、皮膚や腸管の幹細胞でも類似の挙動が見出されています。広く幹細胞に共通してみられる性質かもしれません。
幹細胞が生まれる時、ポテンシャル幹細胞からの「若返り」が起こるのか、あるいは、対称分裂によって2つの幹細胞が生まれるのか、疑問は尽きません。
Nakagawa et al., Developmental Cell, 2007
Klein et al., Cell Stem Cell, 2010
プレスリリース
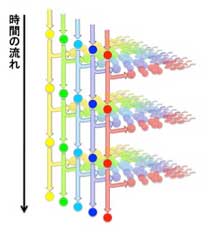
図4 一般的に考えられている幹細胞のふるまい
幹細胞が常に非対称分裂し、幹細胞と分化細胞を生み出すとした場合のモデル。幹細胞のオリジナルが常に保存される結果、すべての系譜はとだえることなく一定の数の精子を作り続ける。
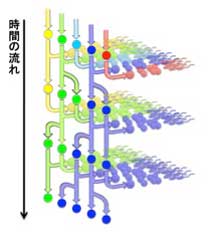
図5 明らかになってきた幹細胞のふるまい
幹細胞は頻繁に失われ、隣の領域の幹細胞から生まれた(コピーされた)幹細胞と頻繁に置き換わる。実際の細胞分裂のパターンは未解明である。
3.精子形成幹細胞のニッチの正体は?
一般に、幹細胞が正常に機能するためには、特殊な微小環境(ニッチ)における制御が不可欠と言われます。しかし、多くの幹細胞系において、ニッチの構造と機能は、未だ謎に包まれています。これは、マウス精子形成でも例外ではありません。私たちは、「未分化型精原細胞」をGFPにより可視化し、その精巣内のふるまいをタイムラプス連続観察する系を確立しました。その結果、未分化型精原細胞は、精細管のなかで、血管や男性ホルモン産生細胞(ライディッヒ細胞)に近い領域に局在し、分化とともにここを離れて精細管全域に散らばっていく事が分かりました(図6)。我々は、この血管に近接した領域を、未分化型精原細胞の増殖と分化を制御する「ニッチ」であると提唱しています(図7)。今後、この「ニッチ領域」の機能と、それを担う分子機構を明らかにし、「真の幹細胞」を制御するニッチ領域とその制御機構の解明を目指しています。
Yoshida et al., Dev. Biol. 2004
Yoshida et al., Science, 2007
プレスリリース(京都大学)
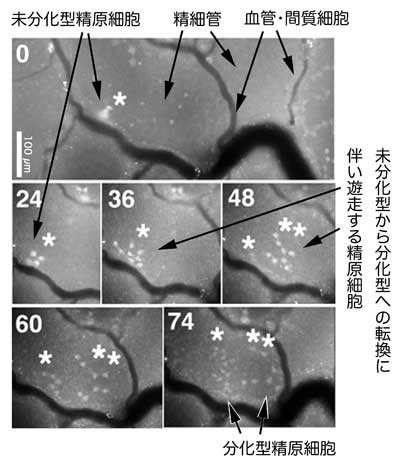
図6 未分化型精原細胞の精巣内ニッチと分化に伴う移動
蛍光標識した未分化型精原細胞の精巣内ライブイメージング。未分化型制限細胞は、血管や間質に近い「ニッチ領域」に局在し、分化に伴ってこの領域から離れ、精細管の基底領域全体に広がっていく。数字は観察時間(時)。
(Yoshida eta al., Science 2007参照。生化学 80 9-13 (2008)より転載)。
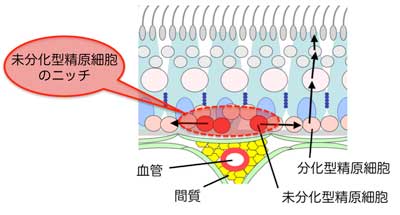
図7 我々が提唱するマウス未分化型精原細胞のニッチのモデル
精細管自体は特別の構造を持たないが、精細管周囲の血管や間質との位置関係にもとづいてニッチが規定される。すなわち、未分化型精原細胞は精細管の中でも、血管・間質に近接する「ニッチ領域」に局在し、分化に伴って精細管全体に広がる。その後体細胞分裂を繰り返したのち減数分裂に入ると、管腔側コンパートメントに移動し、精子に至る分化過程を進む。