2009年 11月20日
幹細胞の居場所(ニッチ)の広さを決める糖タンパク質の働きを解明
私たちの体は数多くの細胞から作られており、それらの細胞は日々、傷害や老化、新陳代謝などにより失われています。それでも私たちの体が無くならない訳は、幹細胞と呼ばれる細胞が元になって、新たな細胞を供給する仕組みがあるからです。岡崎統合バイオサイエンスセンター/基礎生物学研究所の林良樹助教、ミネソタ大学の中藤博志准教授らからなる研究グループは、ヘパラン硫酸プロテオグリカン(以下、HSPG)と呼ばれる糖タンパク質が、幹細胞の維持に必須であることを新たに発見しました。HSPGはタンパク質の本体から糖の長い鎖(糖鎖)を複数伸ばした構造をしています。研究グループはHSPG遺伝子が壊れたショウジョウバエの突然変異体を用いて、精子や卵をつくりだす幹細胞(生殖幹細胞)の様子を観察しました。その結果、HSPGが失われると幹細胞は維持されずに消失してしまうことがわかりました。また研究グループは、HSPGが、幹細胞の維持に必要な拡散性タンパク質の作用範囲を制御しており、この仕組みが幹細胞の居場所(ニッチ)の広さを決めていることを示しました。HSPGはショウジョウバエのみならず、私たち人間を含む多くの動物種において存在しています。本研究の成果は、私たちの体内おける幹細胞維持のメカニズムに重要な知見を提供するものであります。また、幹細胞移植医療において不可欠な、体外での幹細胞の培養や、移植された幹細胞の体内における適切な制御において重要な基礎的知見を提供するものであり、応用医療まで含めた幅広い研究分野において重要な基礎になるものと期待されます。この成果は2009年11月17日(米国時間)、米国の細胞生物学専門誌The Journal of Cell Biologyに掲載されました。
[研究の背景]
幹細胞とは、私たちの体を構成する様々な組織中に存在し、組織を構成する細胞を継続的に生み出すことが出来る細胞です(図1)。このような幹細胞は、私たちの体の維持には不可欠であり、基礎生物学から応用医療まで含めた多くの研究者の興味を惹き付けてきました。
近年、幹細胞が体内で維持される仕組みについての研究が精力的に行われ、幹細胞の維持は、幹細胞のまわりの細胞が分泌する拡散性のタンパク質が行っていることが明らかになってきました。この拡散性のタンパク質は分泌されたのち、組織内の特定の場所にとどまり、そこに幹細胞の居場所(ニッチ)を形成すると考えられています。つまり体内で適切な数の幹細胞が、安定して存在するためには、このようなタンパク質の拡散範囲が適切に制御されなくてはいけないのです。しかし、幹細胞維持において、このような拡散性タンパク質の分布を制御するメカニズムはまったく不明でした。
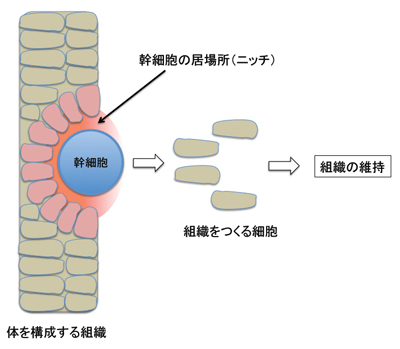
図1:幹細胞の役割
[研究の成果]
研究グループは、ショウジョウバエの卵や精子の元になる細胞の幹細胞(生殖幹細胞)をモデルとして、幹細胞維持における拡散性タンパク質の分布を制御するメカニズムの解明を試みました。その結果、ヘパラン硫酸プロテオグリカン(HSPG)と呼ばれる糖タンパク質が重要な働きをもっていることを明らかにしました。
HSPGはタンパク質の本体から糖の長い鎖(糖鎖)を複数伸ばした構造をしています。HSPGは細胞の外側で、拡散性のタンパク質を糊のようにくっつけて、その分布を制御します。(図2)。研究グループは、HSPGを作り出す遺伝子が壊れたショウジョウバエの突然変異体に注目し、生殖幹細胞の様子や拡散性タンパク質の作用範囲を、レーザー顕微鏡を用いて観察しました。その結果、HSPGが失われたショウジョウバエでは、拡散性タンパク質の作用が失われ、幹細胞は維持されずに消失してしまうことが明らかになりました(図3)。また、反対に、過剰な範囲でHSPGを作り出す様に遺伝子操作したショウジョウバエでは、拡散性タンパク質の作用範囲が広がり、幹細胞の数も過剰になることが分かりました。これらの結果より、研究グループは、生殖幹細胞の制御において、HSPGが幹細胞維持に必須な拡散性タンパク質の作用範囲を決めており、この仕組みによって幹細胞の居場所(ニッチ)の広さが決まることを見いだしました。これはニッチの広さがどのように決まっているのか、その分子メカニズムを明らかにした最初の発見です。
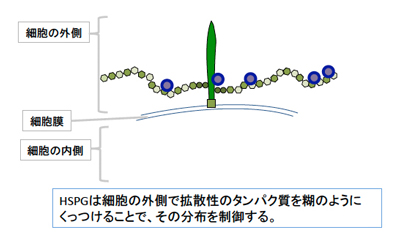
図2:ヘパラン硫酸プロテオグリカン(HSPG)とその働き
HSPGはショウジョウバエのみならず、私たち人間も含めた多くの動物において存在することが知られています。また幹細胞維持のシステムは私たちの体を構成する様々な組織中に存在しています。本研究の成果は、生体内における幹細胞の適切な制御がどのようになされているのかについて重要な知見を提供するものであります。また生体内における幹細胞制御の理解は、近未来的に到来が予想される幹細胞移植医療においても不可欠であり、本研究の成果は、応用医療まで含めた幅広い研究分野において重要な基礎になるものと考えています。
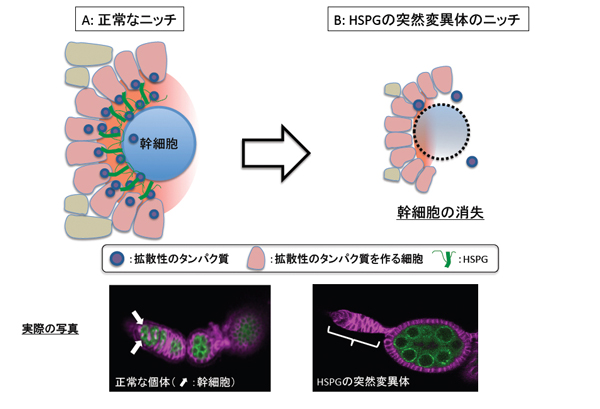
図3:幹細胞のニッチにおけるHSPGの働き
上図:HSPGが無いと、拡散性タンパク質の作用が失われ、生殖幹細胞は維持されずに消失してしまう。下図:ショウジョウバエ生殖幹細胞の実際の様子。写真は正常(左)およびHSPGを失ったショウジョウバエ(右)の卵巣の一部を示している。正常なショウジョウバエでは卵巣の先端に矢印で示した幹細胞が確認できるが、HSPGを失ったショウジョウバエでは、卵巣の先端から生殖幹細胞が失われて中身が空っぽの様子が観察される(括弧で示した部分)。
[発表雑誌]
細胞生物学専門誌
The Journal of Cell Biology (ジャーナル オブ セルバイオロジー)
オンライン版 2009年11月16日号にて発表
論文タイトル:
"Drosophila glypicans regulate the germline stem cell niche"
著者:Yoshiki Hayashi, Satoru Kobayashi, and Hiroshi Nakato
[研究グループ]
本研究は岡崎統合バイオサイエンスセンター/基礎生物学研究所の林良樹助教、小林悟教授、米国ミネソタ大学の中藤博志准教授からなる研究グループによる成果です。
[研究サポート]
本研究は、文部科学省科学研究費補助金 新学術領域研究(配偶子幹細胞制御機構)および米国NIH科学研究費のサポートのもとに実施されました。
[本件に関するお問い合わせ先]
基礎生物学研究所 発生遺伝学研究部門
助教:林良樹(ハヤシ ヨシキ)
Tel: 0564-59-5876(研究室)
E-mail: yoshikih@nibb.ac.jp
URL: http://germcell.nibb.ac.jp/wp/
[報道担当]
基礎生物学研究所 広報国際連携室
倉田 智子
Tel: 0564-55-7628
E-mail: press@nibb.ac.jp
