核には細胞膜や細胞質とは異なったイノシトールリン脂質(PI)シグナル系が存在する。特にホスファチジルイノシトール二リン酸(PIP2)の核内における分布と量的変化は、細胞分裂、分化、細胞死などの諸現象と密接に関係していると考えられている。我々はPIP2の分解酵素であるホスホリパーゼC(PLC)δ1が細胞質と核内との間を行き来することを報告してきたが、今回、核内に蓄積するためのシグナルについて検討した。
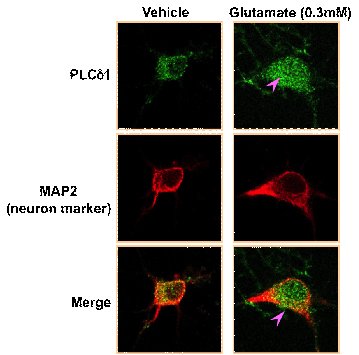
種々の培養細胞を使用して、GFP-PLCδ1および内在性PLCδ1の細胞内分布の解析を行った。PLCδ1は無刺激状態では細胞膜と細胞質に分布するが、Ca2+イオノホアなど細胞内Ca2+濃度の急激な上昇を伴う薬剤処理により、核内に移行した。この際、PLCδ1はインポーチンαに結合することなく直接インポーチンβと結合し、この複合体形成と核内移行にはPLCδ1の活性中心へのCa2+結合が必要であった。さらにラット海馬由来神経初代培養細胞を用いた実験系で、上記薬剤処理による急激なCa2+濃度上昇や高グルタミン酸添加による虚血性神経細胞死誘導に伴ってPLCδ1の核内移行が観察された(右図参照)。また、これらのストレス誘導細胞死の前段階である核収縮にPLCδ1活性が関与することが明らかになった。
さらにPLCδ1遺伝子ノックアウトマウスの胎性線維芽細胞を用いて、PLCδ1遺伝子再導入による細胞増殖に対する影響を調べたところ、対照細胞であるGFPのみを発現させた細胞と比較して、GFP-PLCδ1あるいは核標的化GFP-PLCδ1を発現させた細胞で増殖が抑制されることが判明した。
これらの結果は、これまでに報告されている細胞株におけるPLCδ1遺伝子ノックダウン実験の結果とは異なり、PLCδ1の核移行が増殖抑制あるいは細胞死の前段階として働く場合があることを示唆している。
|