《 基礎生物学研究所要覧 》細胞生物学研究系
|
| DIVISION OF BIOENERGETICS |
|
外界の栄養源が枯渇したとき細胞は自己の構成成分をリソソーム/液胞内で分解する。このオートファジーと呼ばれる細胞応答は,真核細胞に普遍的である。我々の肝細胞では、空腹時に活発なオートファジーが誘導され,血糖値の維持が計られている。酵母細胞では,窒素源の枯渇を引き金として胞子形成という細胞分化が誘導され,このとき既存のタンパク質の大規模な分解が不可欠である。このような細胞内のバルクなタンパク質分解の主要な経路であるオートファジーは,高度に組織化された過程であるに違いない。1955年にリソソームが発見されて以来,細胞内分解コンパートメントの役割と分解機構は,多くの研究者の興味を駆り立ててきたが,まだ多くのことが謎である。その理由はオートファジーを検出する方法がなかったこと,リソソーム系を構成する膜系が複雑かつダイナミックなために,解析の手がかりが得られなかったことによる。
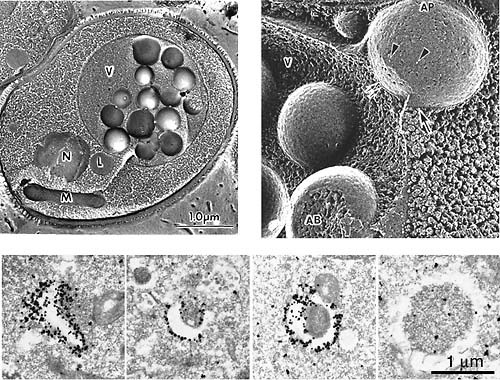
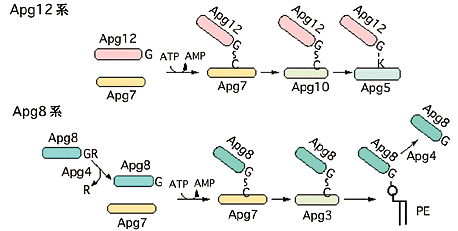
1.酵母のオートファジーの発見我々は,酵母細胞が種々の栄養飢餓に応答して自己の細胞質成分を液胞に送り込み分解すること,その機構が高等動物細胞で広く知られていたオートファジーと同様な複雑な膜現象によることを見いだした(図1)。酵母のオートファジーはN,C,S, リン酸など様々な飢餓によって誘導される。飢餓シグナル伝達経路の解明は未解決の重要課題である。最近我々はホスファチジルイノシトールキナーゼのホモログであるTorキナーゼが栄養源の関知に重要な役割をになっていることを見いだし,その下流因子の同定を進めている。 オートファジーをめぐる最大の問題はオートファジーに伴う大規模な膜動態の機構の解明である。オートファゴソーム形成は細胞内に新たに閉じたコンパートメントを形成する機構であり,いまだ解明されていない膜現象である。細胞質の一部を取り囲む二重膜の構造体,オートファゴソーム膜が何に由来し,どのように形成されるか,オートファゴソームがいかにして液胞/リソソームと特異的に融合するか,オートリソソーム内でなぜオートファジックボディ膜が容易に分解されるのか,オートファジーがどのように制御されているかなど,興味深い課題に挑戦している。 2.オートファジーに関与する遺伝子群酵母は複雑な過程を分子レベルで理解する上で先導的な役割を担ってきた。我々はオートファジーに関わる分子機構の解明を目的として,オートファジー不能変異(apg)株を多数分離した。これらの株はいずれも飢餓条件下にタンパク分解を誘導できず,飢餓条件下に生存率を維持できない。これらの形質の相補を指標として,現在までにオートファジーに関わる15個のAPG遺伝子を同定した。これらのAPG群はそのほとんどが未知の遺伝子であったが,現在これらの遺伝子産物(Apgp)の系統的な解析が進み,オートファジーにおける個々のタンパク質の機能が明らかになり,そのネットワークが構築されつつある。 3.オートファジーに必須な新しいユビキチン様タンパク質の発見Apgpの内7つのタンパク質が新しいタンパク質結合反応に関与していることが明らかとなった。Apg12pはC−末端のGly残基を介してApg5pの中央にあるLys残基の側鎖とイソペプチド結合を形成する。この結合体の生成はオートファジーの進行に必須である。Apg12pはユビキチンと相同性はないが,その反応はユビキチン経路と類似の反応からなっており,Apg7p,Apg10pはApg12pの活性化と結合反応に関与している(図2)。一方Apg8pは,Apg4pによって末端Argが切断された後,末端GlyがApg7pによって活性化され,特異的E2酵素Apg3pに結合し,最終的に膜リン脂質ホスファチジルエタノールアミンに結合する。これらの全く新しいユビキチン様の反応系はヒトに至るまで真核生物に広く保存されている。
図2.Apg12pシステムとApg8pシステム 4.2つのキナーゼ複合体Apgの解析から、酵母オートファジーには2種類のキナーゼが関与することが明らかになった。一つはApg1pを中心としたプロテインキナーゼ複合体である。このキナーゼ活性は,オートファジーの誘導に伴いその調節サブユニットの結合解離を介して調節されている。もう一つはVps34pホスファチジルイノシトール3キナーゼ複合体である。細胞内の様々なプロセスに関わるVps34p を含むオートファジーに特異的に機能する複合体が存在し,恐らくその膜動態を制御している。 5.酵母から高等動植物へ酵母で同定されたAPG遺伝子の多くは、高等動植物にもホモログが存在する。哺乳動物のApg8ホモログであるLC3は動物細胞オートファゴソームの初めてのマーカータンパク質として多くの解析に用いられている。また、我々はAGP5ノックアウトES細胞を構築し, Apg12結合系が哺乳動物でもオートファジーに必須であり,オートファゴソームの前構造である隔離膜の伸長に関わっていることを見いだした。さらにApg5を蛍光標識することによって、生きた細胞の中で球状のオートファゴソームが徐々に形成されていく様子を実時間観察することにも成功した。 細胞にとって必須な細胞内分解の機構は多細胞系でさらに複雑で,高等真核生物に固有の機構や制御系が存在し,オートファジーは栄養飢餓応答,細胞分化における細胞の再構築,細胞死,老化などの過程で様々な役割を担っていると考えられる。植物の生活環では,液胞での分解は重要な役割を果たしていることが予想され,実際APG遺伝子を欠損したシロイヌナズナは,飢餓応答に異常をきたし,枯死の進行が促進されることが明らかになった。一方,マウスを用いた個体レベルでのオートファジーの網羅的観察、APG遺伝子破壊マウスの作成・解析も進行している。 6.オートファジーの更なる理解を目指して細胞内分解コンパートメントにおける分解機構は,バルクな分解のみならず選択的な酵素やオルガネラの除去機構として機能することも予想されている。また,オートファゴソームが関与するマクロオートファジーとリソソーム/液胞膜の陥入によるミクロオートファジーと呼ばれる2つの機構が存在する。近年APG遺伝子群がミクロオートファジーにも必要であることが示されつつある。これらを統合したモデルが構築される必要がある。 参考文献
|
| Copyright(C) National Institute for Basic Biology (webmaster@nibb.ac.jp) | ||